华尔街见闻
分子检测商康为世纪科创板IPO冲刺上会 “无证试剂”检测十万人合规性争议待考
作者: 郑敏芳
研究还是诊断
又一家新冠检测相关的企业来了。
江苏康为世纪生物科技股份有限公司(下称康为世纪)的科创板IPO即将于5月10日迎来上市委的关键审议。
2021年9月30日才向上交所递交科创板IPO申请的康为世纪,在一众新冠检测商中并不算早。据信风(ID:TradeWind01)的不完全统计,除了康为世纪外,2020年1月以来,已经有9家与新冠检测相关的企业成功登陆科创板。
康为世纪此次IPO计划发行不超过2329.03万股以募集9.86亿元,投向“医疗器械及生物检测试剂产业化”、“康为世纪营销网络建设”、“分子检测产品研发”以及补充流动资金。
在疫情所带来检测需求的激增下,主营业务为核酸试剂保存剂等分子检测产品的康为世纪,营收从2019年的0.74亿元“暴增”至2021年的3.38亿元,同期归母净利润也从0.09亿元增长至1.26亿元。
但是这一增长正在面临双重挑战,一方面,康为世纪的新冠病毒核酸检测试剂盒目前尚未获得国内相关部门的注册批文,在国内核酸检测普遍降价的压力下,后续入场新冠核酸试剂市场的康为世纪或很难从中再“分一杯羹”。
另一方面,康为世纪的核心产品——幽门螺旋杆菌产品在尚未拿到注册批文的情况下,被用于部分区域数万人次的幽门螺旋杆菌筛查。康为世纪在问询函中解释称该试剂仅用于科研,但是信风(ID:TradeWind01)调查发现该产品的检测结果或许已被用于诊断治疗及指导,这是否会给其IPO的合规性带来挑战,或许有待上会结果揭晓。
错失的新冠检测业务
作为一家分子检测商,康为世纪则是国内少数实现了“核心酶原料+试剂盒+检测服务”一体化布局的生物科技企业。
分子检测的生产链条具体可以分为分子检测原料、核酸保存、核酸提取纯化、分子诊断试剂盒和分子检测服务。
康为世纪的产品不仅包括分子检测酶原料、核酸保存试剂等,还提供核酸检测服务。
在疫情所带来检测需求的激增下,原本还处于千万量级营收规模的康为世纪,也在报告期内实现了数亿元亿元的营收。
招股书显示,2019年至2021年,康为世纪营收分别为0.74亿元、2.33亿元和3.38亿元,同期归母净利润分别为0.09亿元、1.08亿元和1.26亿元。
与新冠检测相关的业务无疑是这一增长的重要动力。
据信风(ID:TradeWind01)对康为世纪新冠检测相关产品收入的合并统计,2020年至2021年,康为世纪从新冠检测业务中所获得的收入分别为1.43亿元、1.99亿元,占当期收入的比重分别为61.37%、58.88%。
值得注意的是,虽然康为世纪进行了全链条的布局,但是其新冠检测业务的收入主要来源于新冠核酸试剂的上游环节——口腔样本核酸保存试剂和病毒样本磁珠法提取纯化试剂。这两项业务在2021年为其带来了1.29亿元的营收,占当期收入比重达到37.99%。
但在备受关注的新冠核酸检测试剂盒的产品上,康为世纪迄今为止尚未拿到国内的注册批文,其目前用于新冠检测的核酸试剂盒则主要来自于外购。
不过康为世纪表示,新冠病毒核酸检测试剂盒在境内已进入注册检验阶段,预计将于2022年完成临床评价和注册审批
虽然如此,但对于入场看似有些“迟到”的康为世纪来说,核酸常态化以及集采所带来的价格压力无疑会成为后续挑战。
以广东省为例,2022年4月29日,广东省的新冠核酸检测试剂的最低中标价已经降至3.2元,相比于其2020年5月最低中标价13.08元,降幅已有75.54%。
若从营收规模上来看,布局于全链条的康为世纪在新冠检测业务中所获得的收入,与同业公司比起来并不算高。
以被康为世纪列为可比公司的诺唯赞(688105.SH)为例,其2020年来自新冠检测试剂盒的销售收入达到5.19亿元,占当期营收的比重33.18%。
再如康为世纪的可比公司菲鹏生物股份有限公司,其2020年从新冠检测业务中获得的收入高达6.97亿元,占当期营收的比重为65.44%。
值得一提的是,虽然康为世纪的多款产品早已拿到欧盟的注册批文,但是其境外市场表现平平。
招股书显示,2019年至2021年,境外市场为康为世纪带来的营收分别为0.01亿元、0.27亿元盒0.48亿元,占当期营收的比重分别为1.52%、11.38%和14.12%。
境内市场的注册批文尚具不确定性,境外市场开拓不力,康为世纪未来要面临的挑战并不小。
“无证试剂”研究变诊断?
康为世纪还存在部分产品虽未拿到批文,但实际已投入使用的情形。
例如在2021年,康为世纪向泰州医药高新区(高港区)卫生健康委员会提供幽门螺杆菌核酸检测和结直肠癌早期筛查技术服务,并获得了0.50亿元的收入,这笔收入占康为世纪的当期营收比重为14.79%。
上述服务合计共在大众人群中完成共计10万人份的检测,这也是康为世纪在该产品上获得的一份较具规模的数据样本。
康为世纪称这是国内首次有计划、有组织的进行大众人群粪便样本的相关疾病研究工作。
据介绍,康为世纪的幽门螺杆菌核酸检测采用的样本是粪便,其最大的优势在于能够检测幽门螺杆菌的耐药性。
“目前幽门螺杆菌阳性患者的用药习惯仍为经验性用药为主,医生一般选择铋剂+PPI抑制剂+两种抗生素的四联疗法,其中两种抗生素的选择是四联疗法的最大难点,目前国内居民幽门螺杆菌阳性率已达40%-50%,由于缺乏检测手段,医生并不清楚患者体内的幽门螺杆菌对何种抗生素耐药或者对什么药敏感,只能按经验和习惯选择抗生素”。康为世纪表示。
康为世纪进一步指出,其开发的幽门螺杆菌耐药检测产品能够检测目前临床医生常用的两种抗生素:克拉霉素和喹诺酮类,具有较强的特异性和灵敏度。通过对患者所感染的幽门螺杆菌耐药基因的检测可精准指导临床医生合理选择抗生素,从而提高根除率,同时可降低盲目使用抗生素导致的耐药性。
申报材料显示,目前能够对幽门螺杆菌进行耐药性检测的方法一般是医生通过胃镜的临床判断。
这也意味着,康为世纪采用粪便对幽门螺杆菌进行核酸检测的上述方法,具有一定的“体外”优势。
但目前该试剂尚未获得国家食品药监局的注册批文。根据国家食品药监局颁布的《体外诊断试剂注册管理办法》,在中华人民共和国境内销售、使用的体外诊断试剂,应当按照本办法的规定申请注册或者办理备案。
这也意味着,康为世纪在尚未获得批文的情况下,便通过与相关部门的合作,完成了共计十万人次幽门螺杆菌核酸检测。
对于“无证试剂”的问题,上交所也曾提出质疑。
“请发行人说明当地卫健委开展幽门螺杆菌检测及结直肠癌筛查的背景及原因,检测结果的交付对象、交付形式和具体用途,结合前述情况进一步说明相关试剂产品并非用于医疗用途的依据”。上交所表示。
对于“无证试剂”投入使用的合规性质疑,康为世纪曾表示该类活动属于行业惯例。
康为世纪举例称,2021年扬州市邗江区启动了结直肠癌筛查民生工程,分三年对邗江区全区12万名40-74岁的户籍居民免费提供结直肠癌筛查,上海鹍远生物科技股份有限公司(下称鹍远生物)曾作为技术支持方,其采用自主研发的多基因甲基化检测技术对居民进行筛查,而该检测同样未进行备案。
康为世纪同时指出,由于采购方并非医疗器械使用单位,以及相关应用用途为科研,因此并不受到相关规定限制。
“泰州健为(康为世纪的子公司)提供相关技术服务的采购方不属于医疗器械使用单位,泰州健为在服务过程中使用的发行人相关自制研发的科研试剂产品不属于按照规定需要取得注册或备案的情形”康为世纪表示。
但是这一说法或与现实不符,而上述合作也疑似存在“名为科研,实为诊断治疗”的情形。
信风(ID:TradeWind01)注意到,在泰州医药高新区(高港区)的新媒体号——泰州高新先锋所发表的一篇名为《【直击项目一线】健康惠民一号工程:全国首创惠民又惠企》文章中看到,康为世纪所提供的服务数据已被用于提供治疗指导意见。
其中,文章中的健康惠民一号工程正是康为世纪所参与的检测服务。
该文章称:“目前,已在两区5个镇(街道)的43个村(社区)先行试点,覆盖3.8万人。注重做好检测结果运用,针对幽门螺旋杆菌检测阳性的患者,组建技术服务团队,建立患者档案,并分别给出治疗指导意见,做好高危及患病人群治疗、康养等健康管理工作。”
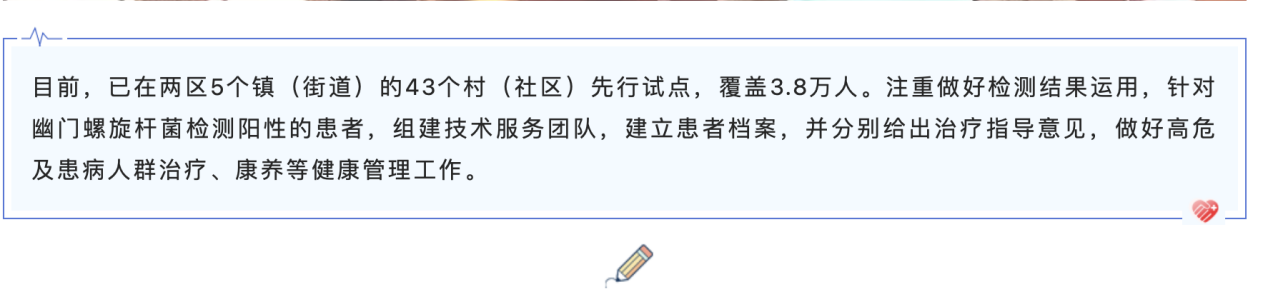 (图片来源:泰州高新先锋的社交平台文章)
(图片来源:泰州高新先锋的社交平台文章)这也给康为世纪的检测合规性问题带来挑战。
事实上,“无证试剂”以科研之名行诊断之时的事件屡见不鲜,此前市场监督管理局便曾对相关公司做出处罚。
以体外诊断试剂行业巨头外企赛默飞为例,其2016年曾被发现对科研用途的试剂——杂草类花粉混合WX5过敏原特异性IgE抗体检测试剂盒(荧光免疫法)进行销售。
彼时赛默飞还曾公开表示产品正式销售前与客户签署了相关科研协议,并明确告知仅限科研项目而不能使用于临床诊断。
但是最终赛默飞还是因以科研为名义进行无证销售遭到了市场监管局的处罚。
反弹行情下的专属投资礼包!投资VIP权益、188元现金红包,100%中奖>>