背水一战的君实生物:2020年度亏损16亿,牵手跨国药企卖PD-1与新冠特效药
崔笑天
中国创新药行业被誉为“10年10倍的黄金赛道”,君实生物、泽璟制药、百奥泰……包括尚在亏损中的Biotech公司纷纷奔赴二级市场。
2月26日,Biotech公司中的“领头羊”——君实生物发布业绩快报。该公司2020年营业收入为15.95亿元,同比增长105.77%;净利润亏损16.72亿元,公司上年同期亏损7.47亿元。
相比2019年,君实生物2020年营收、亏损双双翻倍。对君实生物来说,公司的高光时刻似乎就是登陆A股、站上1300亿市值之时。随后,公司股价在2020年12月触底,如今市值仅为778亿元,蒸发约四成。
天风证券研报认为,目前Biotech公司上市数量显著增多,各家资源禀赋和发展策略差异较大,从企业价值最大化的角度,在Biotech内部将进一步分化,而商业化能力是其中的关键要素。
那么,君实生物何时能扭亏为盈?2021年,PD-1产品的销售能否带动公司“回血?几款“First-in-class”品种是否有望年内上市?与海外药企的合作又将为其业绩增色几分?
PD-1背水一战牵手阿斯利康
君实生物在国内仅有一款药品上市,即PD-1产品——特瑞普利单抗,这也是其业绩的主要增长点。
2020年业绩快报显示,君实生物营收15.95亿元,较上年同期增长105.77%,主要得益于特瑞普利单抗销售收入的增长,以及新增技术许可收入。粤开证券研报预计,在这15.95亿元营收中,特瑞普利单抗的销售收入大约在14亿元左右。
不过,在2021年,特瑞普利单抗注定要面临激烈的竞争——来自君实生物、信达生物、百济神州、恒瑞医药的四款国产PD-1产品均进入国家医保目录。特瑞普利单抗单支价格降幅达到7成以上,这意味着公司需要达到一定的销售量,才能弥补降价带来的利润缩水,抢占稳定的市场份额。
但销售一直不是君实生物的强项。实际上,目前君实生物的销售团队在四家药企中是人数最少的,仅有700人左右,而恒瑞医药的销售团队已达到15000人,二者相距甚远。信达生物、百济神州的销售团队也都分别在千人以上。
强敌环伺,只能背水一战。2月28日,君实生物发布公告称,将特瑞普利单抗在中国大陆地区后续获批上市的尿路上皮癌适应症的独家推广权,以及所有获批适应症在非核心城市区域的独家推广权交给跨国巨头阿斯利康。协议期限为5年。
根据协议,君实生物将支付给阿斯利康一笔服务费,阿斯利康则在特瑞普利单抗尿路上皮癌适应症获批后支付给君实生物一笔首付款,具体金额尚未披露。
阿斯利康是深耕中国市场多年的跨国药企,中国已成为其第二大市场。其年报显示,2020年,阿斯利康总收入达到266.17亿美元,同比增长9%;其中中国区收入占据五分之一,为53.75亿美元,同比增长10%。
值得注意的是,阿斯利康在县域市场的销售能力尤为突出,2020年4月专门成立了“县级肿瘤团队”,团队人数突破4500人。这个数字得到了阿斯利康内部人士的确认,该内部人士告诉《华夏时报》记者,关于特瑞普利单抗的销售,双方正在交接中,但核心市场与非核心市场如何界定,尚不方便对外披露。
在核心市场,双方为何选择尿路上皮癌适应症进行合作?一方面,阿斯利康自家的PD-L1产品——度伐利尤单抗在尿路上皮癌适应症方面的研发受阻。2021年2月,由于上市后的确证性III期DANUBE研究未达到改善总生存期(OS)的主要终点,阿斯利康已经主动撤销该适应症在美国的上市资格,预计也不会再在中国提交该适应症的上市申请。目前度伐利尤单抗国内获批的适应症为非小细胞肺癌。
另一方面,尿路上皮癌也是特瑞普利单抗有望在年内最快获批的新适应症,双方一拍即合。粤开证券研报认为,国际市场,特瑞普利单抗授权 Coherus 获得首付款 1.5 亿美元;国内市场,特瑞普利单抗 2020 年实现 14 亿元销售额,黑色素瘤和鼻咽癌非核心市场的推广权、尿路上皮癌全国市场的推广权授予阿斯利康,将进一步推劢公司未来业绩。但是,特瑞普利单抗依然为君实生物的单一上市品种,在PD-1 竞争愈发激烈的大背景下,未来市场仍存在不确定性。
新冠药物联合疗法在美上市
除了特瑞普利单抗外,君实生物近期还有一款新冠治疗药物——Etesevimab的联合疗法在美获批上市。
2020年5月,君实生物将该药物在大中华地区以外的临床开发、生产和商业化权利授予了礼来。合作协议显示,礼来向君实生物支付1000万美元首付款,并在每一个君实新冠抗体(单用或组合)实现规定的里程碑事件后,向公司支付最高2.45 亿美元的里程碑款,外加该产品销售净额两位数百分比的销售分成。
2021年2月,该药物的联合疗法——Etesevimab及Bamlanivimab双抗体疗法获得美国FDA紧急使用授权,用于治疗伴有进展为重度新冠肺炎及/或住院风险的12岁及以上轻中度新冠肺炎患者。
该授权是基于III期临床试验数据。数据显示,Etesevimab及Bamlanivimab双抗体疗法改善了新冠肺炎患者的症状并使患者住院及死亡风险降低70%,最常见不良事件为输注当天的恶心。
Etesevimab能为君实生物今年的业绩增色几分?
虽然该药物的定价尚未公布,但君实生物方面告诉本报记者,获紧急使用授权后,双抗体疗法拿下了美国政府“大单”——采购10万剂价值2.1亿美元。以此计算,每剂双抗体疗法价格为2100美元,包括Etesevimab1400mg及Bamlanivimab 700 mg。
不过,对于轻中度新冠肺炎患者群体来说,这个价格并不便宜。据本报记者了解,新冠中和抗体药物普遍价格较高,每剂价格集中在1000-3000美元区间。这主要是因为成本难降低。新冠中和抗体药物中蛋白含量极高,新冠疫苗中的蛋白含量以微克计,新冠中和抗体药物则以克计,因此成本也水涨船高。
同时,对蛋白的大量需求也影响了中和抗体药物的产能。相比新冠疫苗年产能动辄达到上亿剂次,中和抗体药物年产能多集中在百万剂级别。礼来在电话会议中透露,公司计划2021年第一季度可以向全球供应25万剂Etesevimab,2021年上半年供应100万剂。
除了价格,还需要注意多款新冠疫苗陆续问世或将对中和抗体药物的销量造成冲击。新冠疫苗的全球接种率在不断攀升。国盛证券研报显示,目前全球接种率约为3.64%,以色列、阿联酋以及英国接种率最高,分别达到98.85%、62.73%、32.33%,欧盟达8.41%。并且新冠疫苗定价较低,集中在10-40美元/剂区间。
国盛证券研报显示,美国已获批上市的两款新冠中和抗体单药的销量不及预期。已分发出去的中和抗体产品仅5%~20%被使用。专家分析其主要原因包括:使用便捷性较差、缺乏数据、重视程度不及预期等。比如,目前中和抗体仅批准用于治疗轻症患者(在首次出现症状的7日内),然而大部分患者会等到病情较为严重的时候才选择就医(主动或被动),因此错过了使用中和抗体治疗的黄金窗口期。
因此,Etesevimab带来的收益存不确定性。这意味着,君实生物2021年的业绩依旧主要靠特瑞普利单抗拉动。君实生物方面表示,该药品近期在国内获批了鼻咽癌的新适应症,亦向美国FDA递交了上市申请,在国产PD-1产品之中属于首个。其进军海外市场速度快于国内竞争对手。
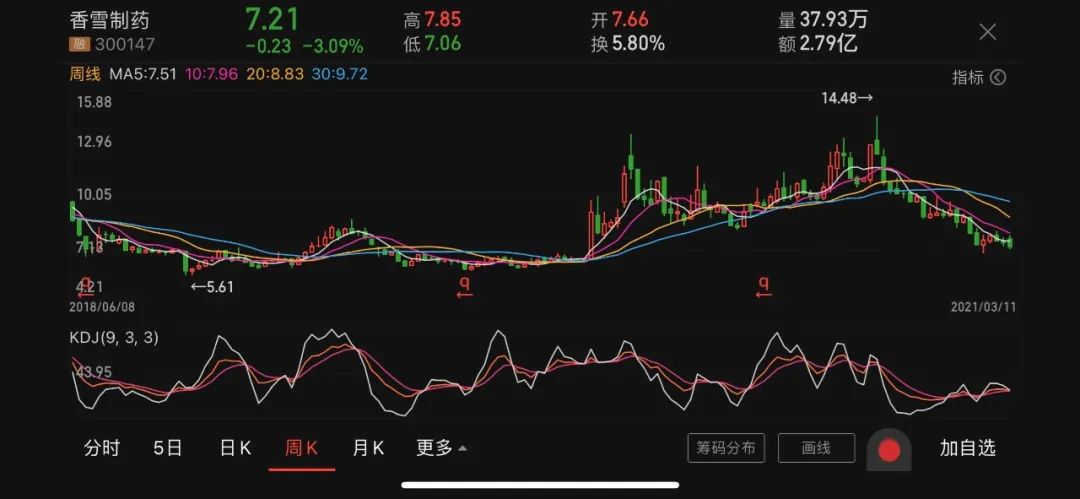
截至3月11日,君实生物收盘价为89元/股,市值达到778.2亿元。自2020年12月股价触底后,君实生物今年公布了一系列利好消息,其股价亦有所回升,但仍与其巅峰时期的超千亿市值存在较大差距。对投资者来说,这或许是一件好事。西南证券研报认为,2021年初以来至今医药行业下跌3.15%,跑输大盘4.14个百分点,高景气赛道的龙头股也在年后经历大幅回调。目前部分大市值龙头平均估值在50-60倍,性价比逐步显现,长期看好具有创新和自主消费的优质赛道的核心资产。