 热点栏目
热点栏目 3月1日,九安医疗(002432.sz)在投资者平台上,对市场传闻“美国食品药品监督管理局准备取消九安医疗ihealth产品的紧急使用授权”进行回应,称该传闻为没有任何事实依据的不实言论,如该言论给上市公司、资本市场造成误导及不良影响,公司必会通过法律手段追究其责任。

之所以有此传闻,据了解,有博拓生物(688767.sh)的专家在浙商证券电话会议中,传播了上述谣言,然而,对此博拓生物也在第一时间回应,经自查,公司未有人员参与浙商证券电话会议。公司已与浙商证券进行了沟通,浙商证券目前正在核实与会人员身份。
对此,浙商证券研究所3月1日盘后向中国证券报记者回应称,目前网络传播的内容属断章取义,专家在电话会议中所述信息或所表述的意见均属于其个人观点,不代表浙商证券研究所观点。
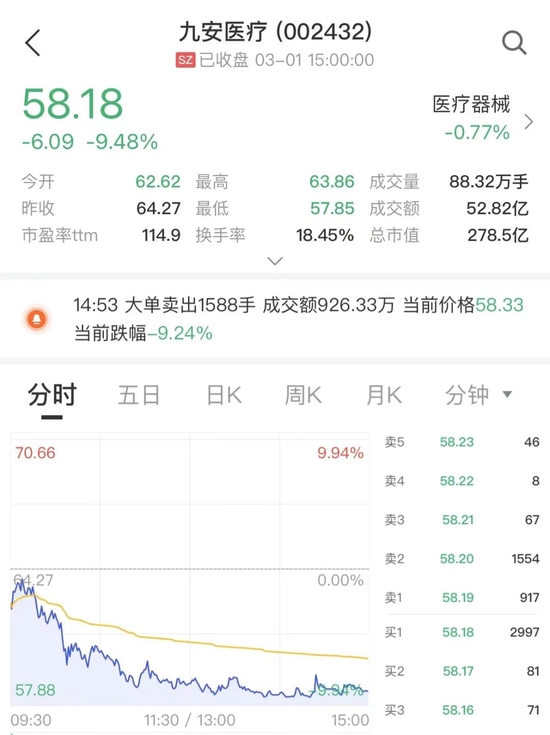
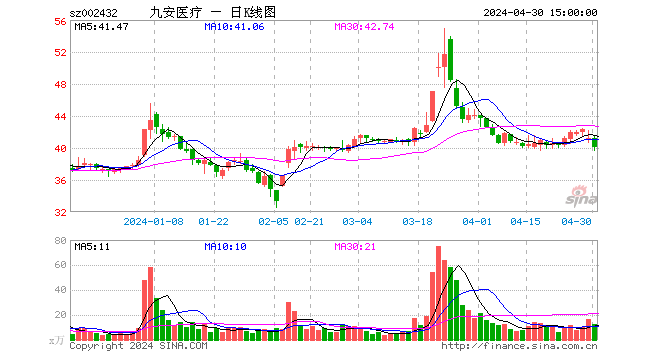
尽管,上述两家上市公司,均迅速否定了传闻。在股价方面,九安医疗可能还是受到了影响。3月1日,九安医疗盘中一度逼近跌停,收盘跌9.48%,报58.18元/股。而博拓生物当日收盘报95.19元,则微涨1.91%。对此,有市场人士表示,自2021年11月开始,九安医疗股价从7元/股左右一路猛涨至最高88.88元/股,涨幅巨大,就算回落至现在的58.18元/股,投资者也是获利丰厚,一有市场传闻传出,股价就大跌也很正常。
不过,在奥密克戎导致疫情升温的背景下,上述两家上市公司的业绩增速仍然飙涨。此前,九安医疗披露业绩预告,预计2021年净利润9亿元至12亿元,同比增长271.4%~395.19%。公司表示,2021年度继续受全球新冠疫情影响,公司新型冠状病毒抗原家用自测OTC试剂盒产品在美国市场销售业绩大幅增长。
博拓生物披露的业绩快报显示,2021年度,公司实现营业总收入18.18亿元,比上年度增长110.09%,实现归属于母公司所有者的净利润8.33亿元,比上年度增长91.32%。
凭EUA授权拿下百亿订单
资料显示,九安医疗成立于1995年,2010年在深交所上市,之前的主营电子血压计和血糖仪等健康类电子产品和智能硬件,疫情前公司营收从未突破10亿元。疫情发生后,公司开始提供新冠抗原家用自测试剂盒。因iHealth新冠抗原家用自测OTC试剂盒产品(iHealth试剂盒),获得美国紧急使用授权,令九安医疗斩获了大额订单。
1月14日,九安医疗公告披露,其美国子公司和美国ACC(U.S.Army Contracting Command,美国陆军合约管理指挥部)签订采购合同,前者向后者销售iHealth试剂盒,合同价税合计金额约为人民币81亿元(含运费),合同已完成签署并生效。根据之前公布的财报,2020年九安医疗全年的营收为20.1亿元,那么上述这一笔订单,可以抵过公司四年的收入。
2月17日,九安医疗再次发布公告称,截至美国当地时间2022年2月15日,公司美国子公司已经就iHealth试剂盒向合同对手方交货共计177139080人份,美国 ACC 陆续向公司美国子公司就69969420人份试剂盒产品支付货款共计3.5亿美元,约合人民币22.65亿元。
截至当地时间2022年2月15日,美国ACC已经累计向九安医疗子公司就91,137,420人份试剂盒产品支付4.65亿美元,上述货款已于美国时间2月16日全部到账,约合人民币29.5亿元。
根据CNBC之前的报道,1月15日起,美国将正式实施新冠快速测试计划。美国政府将免费向民众发送的快速检测试剂(抗原试剂),月需求量或将达到26亿剂,涉及的采购金额或将超过百亿美元。
而要进入上述项目,必须得有美国FDA紧急使用授权(EUA)。2021年11月7日,九安医疗公告披露,其iHealth试剂盒获得FDA的EUA授权,可以在美国和认可美国EUA的国家/地区销售。据公告显示,2021年12月3日至2022年1月10日期间,九安医疗美国子公司分别与美国纽约州卫生部、马萨诸塞联邦及卫生与公众服务部执行办公室,签订了总额约21亿元的iHealth试剂盒订单,再加上美国军方的81亿元订单,近期九安医疗新增合同金额超过100亿元。
据每日商业报道(www.bizvcw.com)了解,目前,美国市场获批的新冠抗原家用自测OTC试剂盒产品共计11家,中国只有九安医疗、东方生物和艾康生物三家公司生产的快速检测试剂,能进入美国市场。此外,美康生物、博拓生物、万泰生物和万浮生物等公司快速检测试剂产品,也正在申请美国的FDA认证。
股民福利来了!送您十大金股!点击查看>>