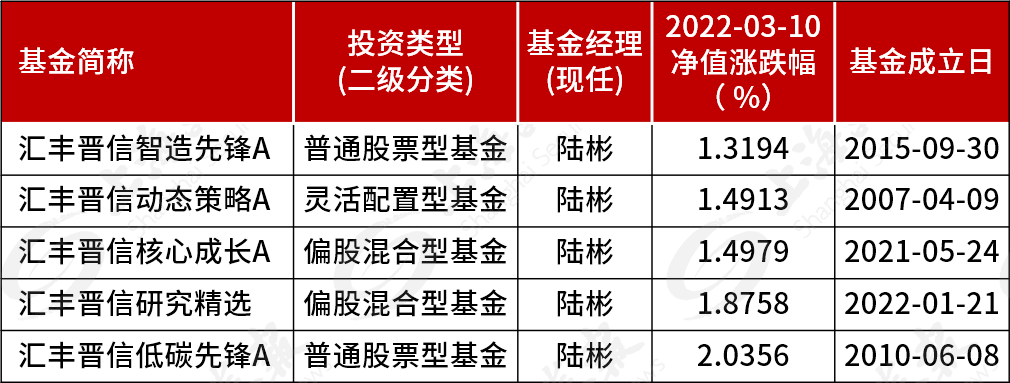
3月11日,国家卫健委发布消息,国务院联防联控机制综合组研究决定,在核酸检测基础上增加抗原检测作为补充,并组织制定了《新冠病毒抗原检测应用方案(试行)》。根据方案,社区居民有自我检测需求的,可通过零售药店、网络销售平台等渠道,自行购买抗原检测试剂进行自测。
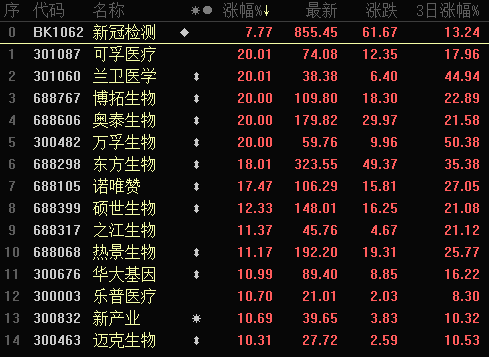
今天午后,新冠检测板块集体直线拉升,截至下午收盘,兰卫医学等5只个股“20CM”涨停,明德生物、九安医疗等多只个股涨停,东方生物、诺唯赞涨超17%。
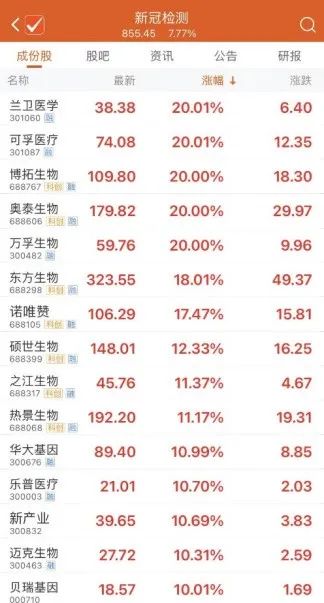 来源:Choice
来源:Choice社区居民可自行购买自测
《方案》规定了抗原检测的适用人群:一是到基层医疗卫生机构就诊,伴有呼吸道、发热等症状且出现症状5天以内的人员;二是隔离观察人员,包括居家隔离观察、密接和次密接、入境隔离观察、封控区和管控区内的人员;三是有抗原自我检测需求的社区居民。
《方案》提出,社区居民有自我检测需求的,可通过零售药店、网络销售平台等渠道,自行购买抗原检测试剂进行自测。
同时,《方案》明确了三类人群进行抗原检测需满足的主要条件、检测试剂的获得渠道,制定了检测发现阳性后的处置管理流程,促进抗原检测与核酸检测相衔接。为便于各地规范开展检测,《方案》还包括两个附件,即基层医疗卫生机构新冠病毒抗原检测基本要求及流程、新冠病毒抗原自测基本要求及流程。

国家卫健委表示,需要说明的是,核酸检测依然是新冠病毒感染的确诊依据,抗原检测作为补充手段可以用于特定人群的筛查,有利于提高“早发现”能力。基层医疗卫生机构具有核酸检测能力的,应当首选核酸检测;不具备核酸检测能力的,可以进行抗原检测,并做好医务人员的培训和患者的沟通指导。隔离观察人员和社区居民进行抗原检测,应当认真阅读说明书、规范操作,一旦抗原检测阳性要立即向有关部门报告;需要时,进行核酸检测予以确认。
实际上,市场对于国内放开新冠居家自测市场已有预期。
无锡市场监管局日前召开家庭自主核酸/抗原检测产品开发座谈会时表示,将继续关注家庭自主核酸/抗原检测产品开发进度,全力指导和服务企业,助推无锡市家庭自主核酸/抗原检测产品尽快上市。
多地升级防控措施
近日,国内出现多点散发本土疫情,引发关注。
国家卫健委3月11日消息,3月10日0-24时,31个省(自治区、直辖市)和新疆生产建设兵团报告新增确诊病例555例。其中本土病例397例,涉及山东、吉林、江苏、甘肃、天津、陕西、河北、浙江、上海、广东、黑龙江、北京、云南、辽宁、内蒙古、河南、青海等17个省市。
部分地区防控措施升级。上海市教委新闻办今日下午公告,3月12日起,本市中小学调整为线上教学,幼儿园、托儿所停止幼儿入园。
吉林省今天召开疫情防控工作新闻发布会通报,3月1日至11日13时,吉林省本轮本土疫情累计报告新冠肺炎确诊病例526例,其中吉林市396例、长春市78例、延边州51例、松原市1例。本轮疫情病毒株为奥密克戎变异株BA.2进化分支,初步判断为2月下旬输入吉林省并在本地传播。目前,吉林市、长春市九台区疫情出现社区传播,处于快速上升期。
发布会通报,全力以赴强化重点部位防控,成立高校专班工作组,强化校园管控、核酸检测、环境消杀、物资生活保障、督导检查等工作,力争在最短的时间内遏制疫情在校园传播。
新冠抗原检测产品
单月市场规模有望超170亿元
新冠检测目前主要基于分子学(遗传物质)和免疫学(蛋白质)形成两大检测路径。西南证券认为,分子学中的RT-PCR由于灵敏性和特异性很高,成本适中,已成为新冠感染判定的金标准,而基于免疫学的新冠抗原的检测虽然灵敏性不及PCR,但特性性和PCR比相差不大,且检测出结果的时间较快(自测产品普遍15-30分钟),成本也低,比较适合做新冠阳性患者的筛查。
国内目前暂时还未批准新冠抗原家用自测的产品上市,已上市的5个新冠抗原皆为医疗机构端使用,除了最新获批的诺唯赞试剂盒,其它四款分别为北京金沃夫生物工程科技有限公司(乳胶法)、华大基因子公司深圳华大因源医药科技有限公司(荧光免疫层析法)、万孚生物(胶体金法)、北京华科泰(荧光免疫层析法)。
西南证券研报显示,主要新冠抗原家用自测试剂盒未来的主要市场预计来自美国、欧盟、日本以及中国,按照总人口和平均检测次数,预计全球市场潜力有望超过500亿美元,其中美国市场占据大头,国内市场有望达到84亿美元。
中泰证券表示,预测国内单月市场规模或为177亿-266亿元。如考虑到居民、企业自费购买情况,预计新冠抗原检测产品采购需求有望进一步提升。
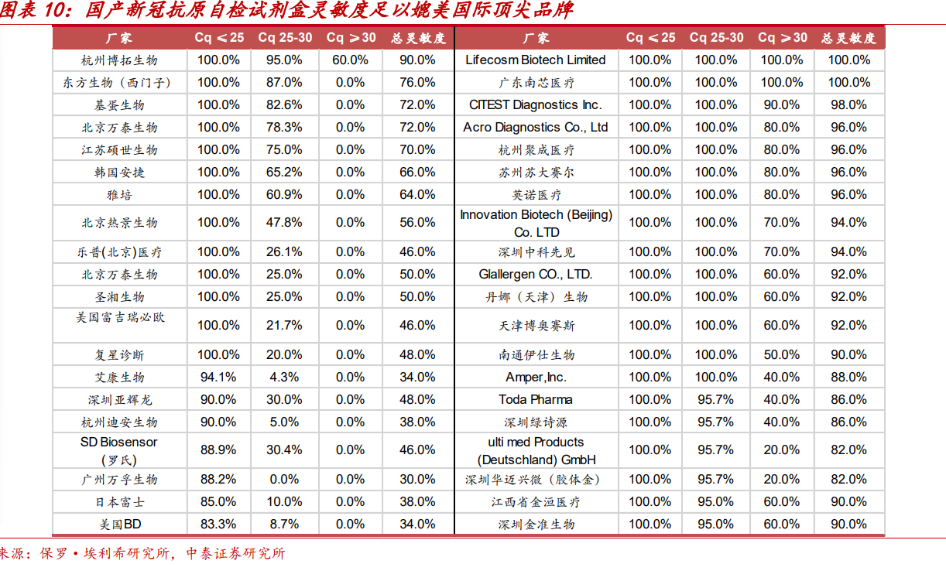 图片来源:中泰证券
图片来源:中泰证券多家上市公司发布相关公告
3月11日晚间,多家上市公司就新冠病毒抗原检测产品发布公告。
亚辉龙公告,截至目前,公司的新冠病毒抗原检测产品尚未取得国内药品监督管理部门颁发的注册证书。
诺唯赞公告,全资子公司诺唯赞医疗自主研发生产的新型冠状病毒抗原检测试剂盒近日收到国家药监局颁发的《医疗器械注册证》。
热景生物公告,公司近日获得新加坡卫生科学局(HSA)批准新冠抗原检测试剂一项,产品名称为北京热景生物科技新型冠状病毒2019n-CoV 抗原检测试剂盒(前鼻腔)。该产品获得HSA认证批准后,可在新加坡和认可新加坡(HSA)认证的国家及地区进行销售。
东方生物公告,截至目前,公司新冠抗原检测试剂尚未取得国内认证证书,请投资者理性预判。
投资避险工具看这里,低风险理财、7%+收益、0手续费>>